高分子溶液・ゲル研究グループ
溶液中の高分子電解質
当研究グループの研究の中心的な目的は、溶液中における高分子電解質のコンフォメーションとダイナミクスの物理を理解することです。この課題に対して、私たちは主に散乱法とレオロジー法を用いて取り組んでいます。塩、界面活性剤、非溶媒が共存する高分子電解質系のような複雑な多成分系にスケーリング概念を適用し、構造特性および流体力学的特性を抽出しています。
高分子電解質(PE)は、主鎖に沿ってイオン性基を持つ高分子です。溶液中では、対イオンが解離して高分子は正味電荷を持つため、強く相関した系となります。高分子電解質は関節液中に存在し、関節間の潤滑を担っています。また、食品や医薬クリームではテクスチャー改質剤として働きます。ワインでは酒石酸の結晶化防止のために添加され、洗濯用洗剤では再汚染防止剤および軟水化剤として機能します。近年では、mRRA(高分子電解質の一種)ワクチンが世界規模でCOVID-19に対する免疫化を大きく変革しました。このように生物学的現象や工業製品において非常に重要であるにもかかわらず、高分子電解質はかつてPG de Gennesによって「最も理解されていない凝縮系」と表現されました。この評価は現在でも当てはまります。以下に、当グループが取り組んでいる高分子電解質溶液研究のいくつかのテーマを示します。高分子電解質物理における諸問題の概説については、以下の総説も参照してください。
- 希薄溶液中の高分子電解質, 最近の進展と未解決問題
- 高分子電解質溶液のレオロジー, 現在の理解と展望
- 柔軟な高分子溶液の構造と線形粘弾性, 高分子電解質溶液と中性高分子溶液の比較
- 溶液中および界面における高分子電解質の理論
対イオン凝縮
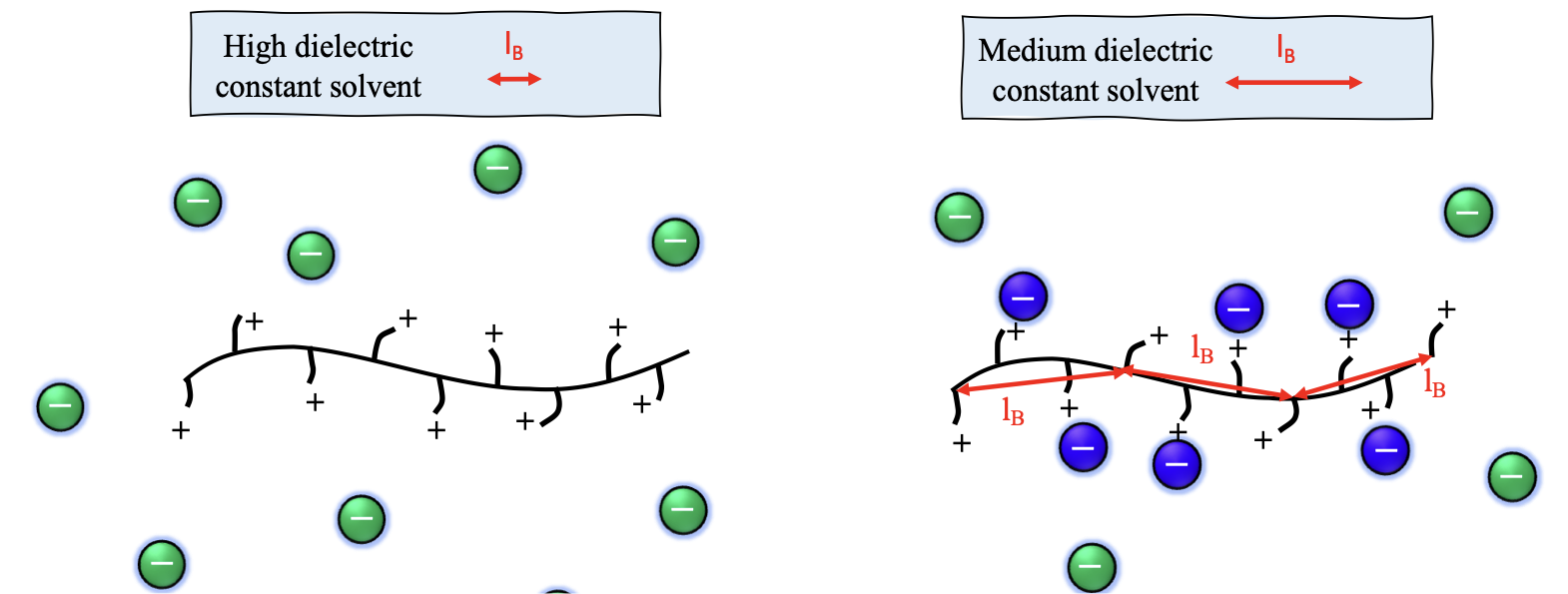
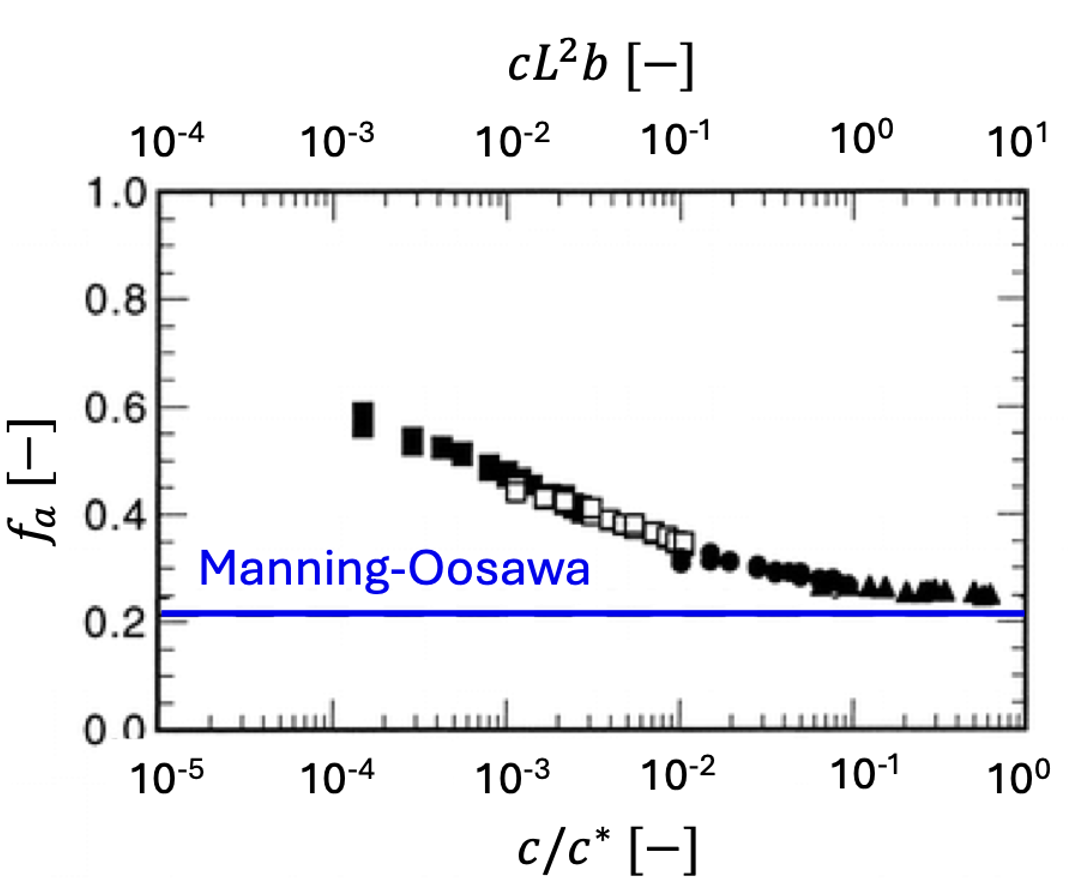
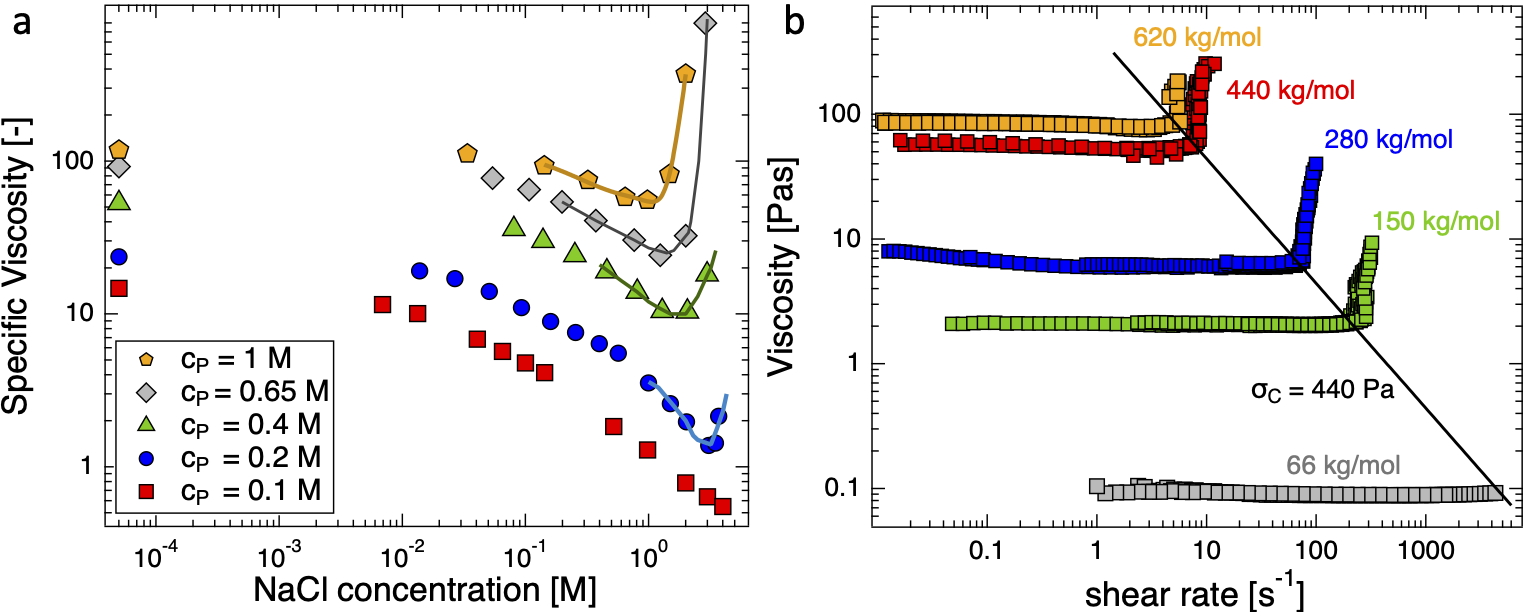
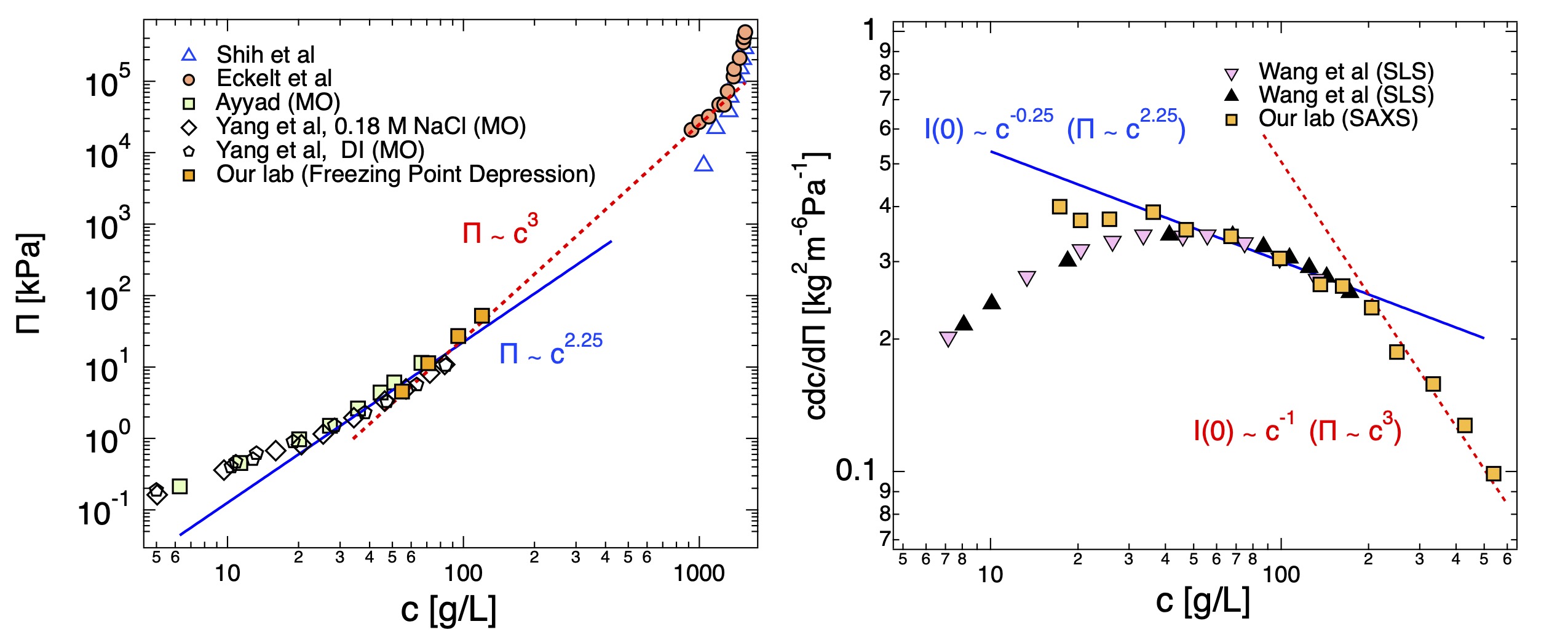
Oosawa-Manning モデルは無限希釈の棒状鎖に対して導かれましたが、図2に示した実験データは、OM のしきい値が重なり濃度 c* 以上(準希薄領域)でのみ適用されることを示しています。c* 未満では、対イオン活量 (\(f_a\)) は希釈に伴って増加します。\(c/c^*\ll 1\) では、Muthukumar および Dobrynin らの予測どおり、これが 1 に達すると期待されます。Tang と Rubinstein は、c^* 以上で Oosawa-Manning の結果を再現する対イオン凝縮モデルを展開しました。
Manning モデルの枠組みでは、凝縮した対イオンの割合 (f) は以下の関数のみに依存するはずです:
\(\ \)
- 荷電基間距離
- 対イオンの価数
- 溶媒のビェルム長
Oosawa–Manning モデルでは、対イオンの種類や、側鎖基および主鎖との非静電的相互作用(例, 疎水性効果)は考慮されていません。
対イオン凝縮と電荷密度: 凝縮した対イオンの割合(および関連パラメータ)の電荷密度依存性については、いくつかの信頼できるデータセットが存在します。これらは Manning により [Manning 1979, Manning 1996, Manning & Ray 1998] でレビューされ、さらに最近では私たちによって [Gharehtapeh et al. 2025] で総説されています。Oosawa–Manning の予測は実験と定性的に一致しています。
現在の文献における大きな制限は、比較的広い系が調べられてきたにもかかわらず、単一の系について複数の手法(例, 電気泳動、オスモメトリー、電気伝導度)で対イオン凝縮が測定されていないことです。利用可能なデータから明らかなように、異なる手法は凝縮した対イオンの割合に対して異なる値を与えます。たとえば、水中 NaPSS に対する自由対イオン分率の浸透圧法、伝導度法、誘電分光法による推定値は [Bordi et al. 2002] で比較されており、約 3 倍の差があります。カルボキシメチルセルロースの有効電荷密度を推定する6つの方法の比較でも同様の不一致が見られました [Gharehtapeh et al. 2025]。これはおそらく、異なる手法が異なるイオン集団を見ているためです。
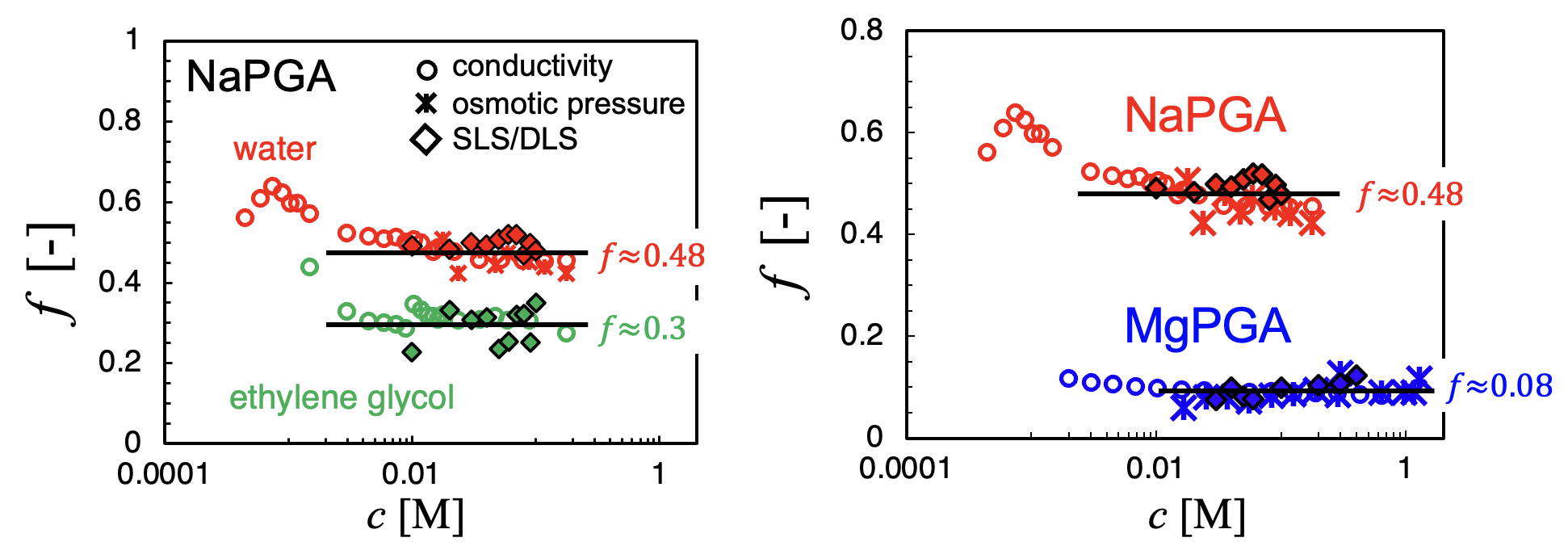
対イオン価数の影響: Rinaudo らによる電位差測定および浸透圧測定の結果を、私たちは [Gharehtapeh et al. 2025] でレビューしました。それによれば、二価対イオンをもつ高分子電解質の有効電荷分率は一価イオン系のおよそ半分であり、Oosawa–Manning モデルと一致しています。三価対イオンに関するデータは、水中で三価高分子電解質塩の溶解性が低いため、いまだ不足しています。Section II では、この制限に対処する新しい結果を示します。
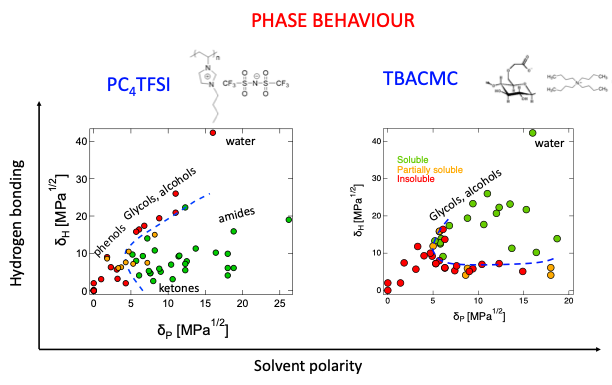
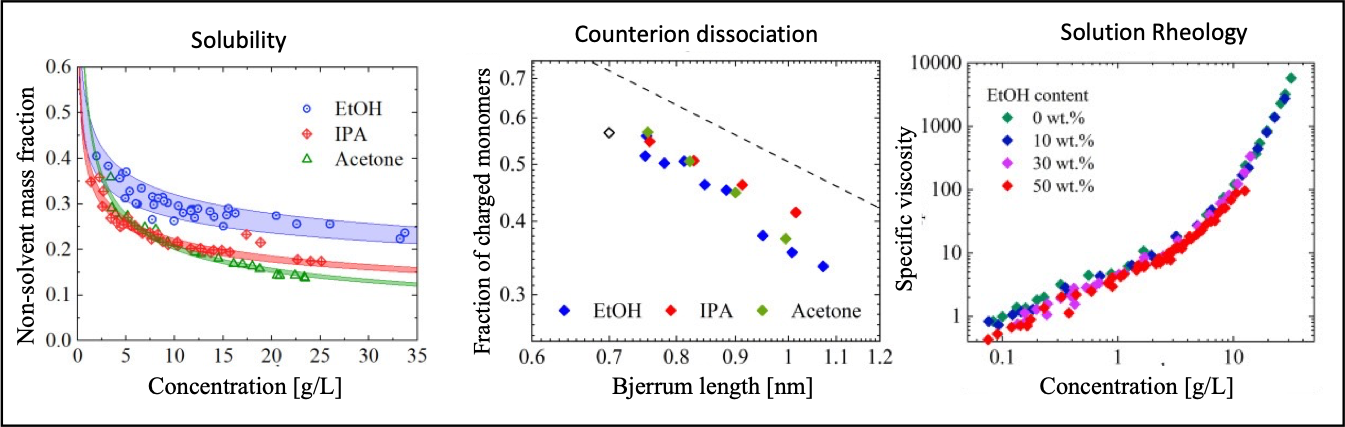
対イオン凝縮とビェルム長: 高分子電解質に関する研究の大半は水系に集中しています。水/有機混合系も研究されていますが、それは狭いビェルム長範囲に限られています [Hou et al. 2025a]。この実験研究の空白の理由は、おそらく有機媒体中での高分子電解質の溶解性が低いことにあります。これについては 以下 を参照してください。 自由イオン分率 (f) のビェルム長依存性を、そのような混合系を除いて直接測定した研究は3件に限られます。そのうち2件は Manning 理論と一致しない結果を与えています。[Lopez et al. 2024] は2種類のポリ(イオン液体)の重なり濃度スケーリングから f を推定し、[Beer et al. 1997] はいくつかの溶媒中における quaternized poly(2-vinylpyridine) の回転半径データに変分モデルを当てはめました。これに対して、より直接的に f を見積もる Gulati et al., 2025 の伝導度測定は、Oosawa–Manning の予測とよりよく一致しています(このプレプリント を参照)。
実際には、信頼できる $f$ の値を得ることは容易ではありません。浸透圧測定は浸透圧に寄与するイオン数を直接見積もる方法ですが、市販のオスモメーターを用いて有機溶媒中の浸透圧を測定するのは困難です。光散乱は、高分子電解質溶液の浸透圧特性を調べるうえで魅力的な手法です。なぜなら、ゼロ角散乱強度が溶液の浸透圧圧縮率に関係しているからです。具体的には、過剰光散乱強度(通常は Rayleigh 比 \(\Delta R\) で表される)は次式で与えられます: \[ \Delta R(q) = K \rho_{\mathrm{pol}}^{2} N_A S(q) \] ここで \(\rho_{pol}\) は高分子密度、\(S(q)\) は全構造因子、\(K\) は光学コントラストです: \[ K = \frac{4\pi^2 n_0^2}{N_A \lambda^4}\left(\frac{dn}{dC}\right)^2 \] ここで \(\lambda\) は光の波長、\(\frac{dn}{dC}\) は屈折率増分です。 ゼロ角における全構造因子は次式で与えられます: \[ S(0) = k_B T \, c \, \frac{dc}{d\Pi} \] したがって、原理的には濃度に対する浸透圧の微分を測定することが可能であり、そこから自由対イオンの割合を得ることができます(\(\Pi \simeq k_BTfc\))。 しかし実際には、この関係を塩無添加高分子電解質に適用することは容易ではありません。というのも、低 $q$ における散乱関数は通常、いわゆる low-$q$ upturn に支配されるからです。この過剰散乱により、ゼロ角強度は溶液の浸透圧圧縮率から予想される値よりも数桁大きくなります。この low$-q$ upturn の起源は理解されておらず、文献中で広く議論されてきました。 最近、私たちは十分に小さい孔径でろ過することにより low-$q$ upturn を大幅に除去でき、さらに動的光散乱(DLS)を用いて slow mode の残存寄与を分離できることを示しました。下図を参照してください。この寄与を除去すると、得られる散乱強度は塩無添加高分子電解質溶液に期待される浸透圧圧縮率に対応することがわかりました。したがって、補正後のゼロ角強度は自由対イオン分率の決定に利用できます。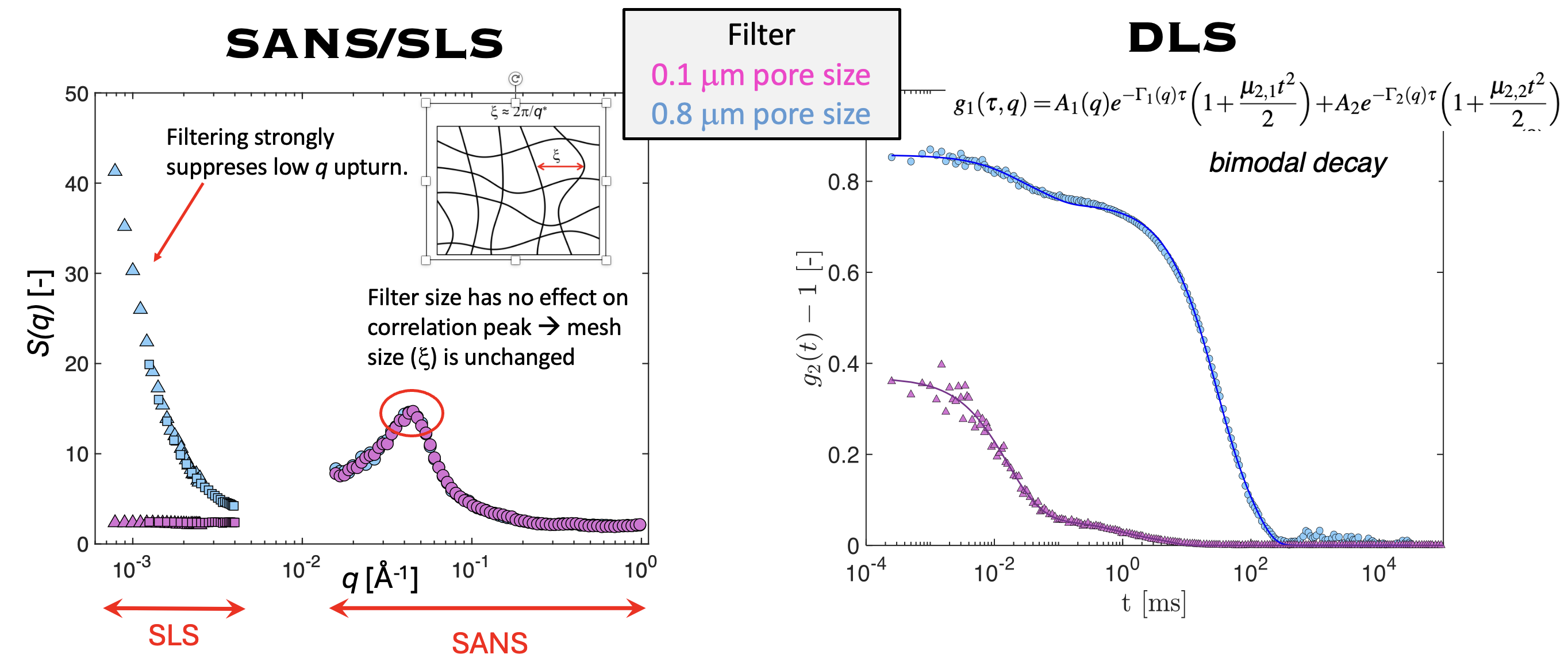
イオン対形成
凝縮層内の対イオン濃度はモル濃度領域に達するため、イオン対が形成され得ます。主として電荷密度、イオン価数、および溶媒の誘電率に依存する対イオン凝縮とは異なり、イオン対形成はイオン周囲の溶媒構造に強く影響されます。したがって、イオン対形成は、高分子電解質溶液、ゲル、膜におけるイオン選択性、相挙動、イオン輸送を含む特異イオン効果を理解するうえで重要です。
私たちの研究では、密度および音速測定を用いてイオン対形成を定量化しています。イオンが高分子上の荷電基に会合すると、水和の変化により系の体積および溶媒の圧縮率に測定可能な変化が生じます。イオン種および濃度に応じた密度と音速の変化を解析することで、イオン対形成の程度とそれに対応する水和変化を評価します。さらに、平衡透析を用いて、異なるイオンが高分子によってどの程度選択的に保持または排除されるかを決定します。これらの手法を組み合わせることで、微視的なイオン対形成と巨視的なイオン選択性を結びつけ、選択的高分子電解質材料を理解し設計するための定量的な枠組みを提供しています。